|
|
International Journal of Arrhythmia 2014;15(2): 33-36.
|
 |
| MAIN TOPIC REVIEWS |
Electrocardiography Changes
after Stroke |

|
|
 |
 |

서론
심장 질환이 뇌졸중과 같은 뇌혈관 질환의 발생에 영향을 미치는 것은 잘 알려져 있으며, 대표적으로 심방세동 환자에서 뇌졸중의 위험성은 5배 정도 높다.1
또한 뇌손상 후에 발생하는 심혈관계의 부작용 역시 비교적 흔한 편이며, 이들에게서 높은 유병률과 사망률을
보이는 것으로 알려져 있다.2 뇌손상 후에 발생할 수 있는 심혈관계 부작용은 매우 광범위하게 벌어질 수 있는데, 단순한 심전도의 변화에서부터 혈압 상승 또는 저하, 부정맥의 발생, 심근 효소의 증가, 일시적인 심기능 부전(stress-induced cardiomyopathy) 또는 심인성
급사에 이르기까지 한다. 따라서 이러한 다양한 변화는 cardiologist와 neurologist의 적절한 판단과 치료를 어렵게 만든다.
뇌손상 환자에서의 심전도의 변화
뇌에서 발생하는 변화는 심전도에 영향을 미친다.
이는 특히 허혈성 뇌졸중보다는 지주막하 출혈(subarachnoid
hemorrhage, SAH)에서 더 빈번하게 관찰된다. 가장 흔한 소견은 ST segment의 변화, T wave의 역전, 뚜렷한 U wave와 QTc interval의 연장 등이다.3
이러한 변화는 뇌손상 후 2-3일 내에 가장 뚜렷하고, 시간이 흐르면서 정상화되어간다. 그러나 일부에서는 8주 이상 심전도의 변화가 지속되는 경우도 있다.
이러한 심전도의 변화는 대개는 심혈관계의 증상을 동반하지는 않지만, SAH 환자에서는 ST segment의 저하나 T wave의 변화는 추가적인 neurologic deficit를 초래하여 결과가 좋지 않거나, 사망률이 높은 것으로 알려져 있다. 또한 QTc interval의 연장이 뚜렷한 경우는 뇌손상 후
발생하는 심인성 급사의 원인이 될 수 있다. 특기할 만한
것은 QTc interval의 연장이 결과가 좋지 않은 환자에서는 지속되었다는 것이다.2
이와 같이 뇌손상 환자에서의 허혈성 심전도 변화는 응급실에서의 적절한 초기 조치를 하는 데 어려움을
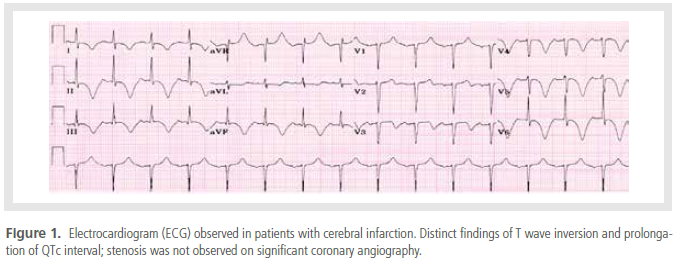
주기도 한다. 다음 그림은 massive cerebral infarction으로 진단된 환자에서 응급실 내원 당시의 심전도이다
(Figure 1). 내원 당시 comatous mentality를 보였으며,
brain CT 상에는 저명한 이상 소견은 관찰되지 않았다.
또한 cardiac enzyme 역시 약간 상승된 소견을 보여 응급으로 관상동맥 조영술을 시행하였으나 유의한 협착
소견은 관찰되지 않았으며, 재차 시행한 brain MRI에서
massive infarction이 진단되었던 경우이다.
이 외에도 심방기외수축, 심실기외수축, 동성서맥 등이 관찰될 수 있으며, 이전에 발견되지 않았던 심방세동이 발생하는 경우도 있다.
특히 색전증에 의해 뇌졸중이 발생된 것으로 의심되는 고령의 환자에서는 입원 후
Holter monitoring을 시행하는 것이 이전에 진단되지
않았던 새로운 심방세동을 진단하는 데 도움이 될 수 있다.4 그 외에도 torsades de pointes와 같은 치명적인
부정맥이 드물지만 발생할 수 있으며, 심근 효소의 증가와
관련이 있는 것으로 알려져 있다.
신경성 심손상(neurogenic cardiac injury)
신경성 심손상의 기전은 뇌손상에 의해 유발된 catecholamine과
neuroinflammatory response에 의한 것으로 여겨진다(Figure 2). 뇌손상이 일어나는 경우 central
neuroendocrine axis에서 catecholamine storm이 유발되며, 특히 insula와 hypothalamus 지역에서의 손상이
자율신경계의 기능 부전과 neuroinflammatory response를 일으키는 것으로 알려져 있다.5 이들은 손상된 뇌병변으로의 혈류를 유지하기 위한 보상 기전으로 여겨지지만,
심혈관계의 손상을 유발하기도 한다.
우선 catecholamine storm에 의한 systemic vasoconstriction이
유발되며, 이들은 심장 후부하(cardiac
afterload), 심근 작업 부하(myocardial workload) 및
산소요구량(oxygen demand)을 상승시킨다. 이에 따라
subendocardial ischemia가 유발될 수 있으며, 심기능의 저하 현상 및 저혈압을 일으킬 수 있다. 이러한 변화들은 심전도상에서 허혈성 변화를 일으킬 수 있는
기전으로 설명될 수 있을 것이다.
또한 과도한 catecholamine storm은 neurogenic
stunned myocardium (NSM) syndrome을 유발할 수
있다. NSM syndrome은 대개 가역적이며, 심전도의 변화, 부정맥, 좌심실 기능 부전 및 심근 효소의 증가를
특징으로 한다. 이는 stress-induced cardiomyopathy (또는 Takotsubo cardiomyopathy)와 유사한 기전으로
설명된다.6 Myocardia sympathetic nerve terminals에서의 과도한 norepinephrine의 분비가 원인으로 알려져 있으며, plasma catecholamine level과는 무관한 것으로
되어있다.7 심근 간질(myocardial interstitium)에의 catecholamine의
방출은 beta-1 adrenergic receptor에 의해
조절되는 칼슘 채널(calcium channel)을 개방하게 되고,
adenosine triphosphate의 빠른 고갈을 유발시켜, mitochondrial
dysfunction 및 cell death를 일으킨다. 이들은
조직학적으로 myocardial contraction band necrosis 소견으로 관찰되며, 이러한 변화는 subendocardial region에 집중되며, 심첨부에는 관찰되지 않아 vascular territory보다는
sympathetic innervation이 되는 territory에서 관찰된다. NMS syndrome에서 심근 손상(myocardial
damage)의 정도는 뇌손상의 중증도와 연관이 있는 것으로 알려져 있으며, 동물 실험에서는 SAH가 발생한 지 4시간 이내에 심근이 손상되는 결과를 보여주었다.8,9
이외에도 뇌손상은 강한 염증 반응을 일으킬 수 있으며, cytokine, adhesion molecules, peptide 등이 뇌로부터 체내 순환계에 방출되어 전신성 염증 반응 증후군(systemic inflammatory response syndrome, SIRS)을
유발할 수 있다. 이는 SAH 후 발생하는 허혈성 뇌손상을 일으키는 원인이 되며, 다발성 장기 손상 및 부정맥
발생의 원인으로 설명될 수 있다.10,11
뇌병변의 위치에 따른 부정맥의 차이
뇌병변의 위치에 따라 부정맥의 발생 양상이 다소 다른 것으로 알려져 있다.12 이는 뇌의 좌반구(hemisphere)와 우반구가 심장의 기능에 미치는 영향이 다르기 때문이다.
동물 실험에 의하면 굴심방결절(sinoatrial node)은 우측 자율신경계의 영향을 받게 되어 우반구의 수질(medulla)이나 시상하부(hypothalamus)를 자극하거나
억제시키는 경우, 좌반구에 비해 심박동수에 영향이 더욱 크며, 우측 insula에 손상이 있는 경우 서맥이나 저혈압이 더욱 잘 발생한다.13 또한 우반구의 손상 시
상심실성빈맥(supraventricular tachycardia)이 더욱 흔한데,
heart rate variability에 의하면 우반구 뇌손상에 의한
parasympathetic tone의 저하로 인한 sympathetic tone의 증가에 의한 것으로 보인다.14 또한 우측 중간대뇌동맥(right middle cerebral artery) 폐쇄에 의한 경우 QT 연장(QT prolongation)이 더욱 흔한 것으로 알려져 있어,
치명적인 부정맥이나 급사가 우반구 뇌졸중에서 더욱 흔한
이유로서 설명된다. 2013년 AHA/ASA 치료 지침에도 뇌경색의 손상의 범위가 크거나 우반구 손상이 있는 환자에서 좀 더 적극적으로 모니터링할 것을 권유하고 있다.15

예후 및 처치
신경성 심손상에 의한 심전도의 변화는 사망률이나
추가적인 뇌손상에 의한 좋지 않은 결과를 가져오는 것으로 알려져 있다. 심전도 변화 이외에도 심근 효소의 증가, BNP level의 증가, 국소벽 운동 장애가 있는 경우에도
예후는 좋지 않다.2 그러나 이들의 변화는 뇌손상의 범위가 연관이 있으며, QTc interval의 연장에 의한 심실성 부정맥이 발생하는 경우가 아니고는 대개는 임상 경과에
큰 영향을 미치지 않는다. 따라서 우선적으로는 뇌손상을 최소화하거나 안정시키는 치료가 우선되어야 한다. 그러나 적절한 치료 방향을 정하고, 임상 성적을 높이기
위해서는 입원 시의 심전도 검사가 필수적이며, 이상이 있는 경우에는 정상으로 돌아올 때까지 지속적인 모니터링이 필요하다. 특히 QTc가 증가되어 있는 환자에서는 QTc를 증가시킬 수 있는 약물의 사용에 더욱 주의를 요한다.
결론
뇌졸중 환자에서 심전도의 변화는 비교적 흔하며, 좋지 않은 결과를 가져오거나 사망률을 증가시키는 것으로 알려져 있다. 이들은 대개 뇌손상이 발생한 후 2-3일
내에 가장 흔한 것으로 알려져 있어 적극적인 모니터링이 필요하다. 그러나 이러한 심전도의 변화는 뇌손상의
범위와 연관이 있으며, 일시적인 변화로 생각된다. 대개는 supportive care만으로 회복되는 경우가 대부분이다
다만 neurogenic stunned myocardium syndrome이 발생하는 경우에는 좌심실 기능 부전 및 심실성 부정맥의 빈도가 높아지므로 투여량 조절에 더욱 주의가 필요하며, QTc를 늘리는 약물의 사용을 금하여야 할 것이다.
References
- Wolf PA, Abbott RD, Kannel WB. Atrial fibrillation as an in dependent risk factor for stroke: The framingham study. Stroke. 1991;22:983-988.
- van der Bilt IA, Hasan D, Vandertop WP, Wilde AA, Algra A, Visser FC, Rinkel GJ. Impact of cardiac complications on outcome after aneurysmal subarachnoid hemorrhage: A meta-analysis. Neurology. 2009;72:635-642.
- Goldstein DS. The electrocardiogram in stroke: Relationship to pathophysiological type and comparison with prior tracings. Stroke. 1979;10:253-259.
- Lazzaro MA, Krishnan K, Prabhakaran S. Detection of atrial fibrillation with concurrent holter monitoring and continuous cardiac telemetry following ischemic stroke and transient ischemic attack. J Stroke Cerebrovasc Dis. 2012;21:89-93.
- Lim HB, Smith M. Systemic complications after head injury: A clinical review. Anaesthesia. 2007;62:474-482.
- Wittstein IS, Thiemann DR, Lima JA, Baughman KL, Schulman SP, Gerstenblith G, Wu KC, Rade JJ, Bivalacqua TJ, Champion HC. Neurohumoral features of myocardial stunning due to sudden emotional stress. N Engl J Med. 2005;352:539-548.
- Banki NM, Kopelnik A, Dae MW, Miss J, Tung P, Lawton MT, Drew BJ, Foster E, Smith W, Parmley WW, Zaroff JG. Acute neuro cardiogenic injury after subarachnoid hemorrhage. Circulation. 2005;112:3314-3319.
- Tung P, Kopelnik A, Banki N, Ong K, Ko N, Lawton MT, Gress D, Drew B, Foster E, Parmley W, Zaroff J. Predictors of neurocardiogenic injury after subarachnoid hemorrhage. Stroke. 2004;35:548-551.
- Masuda T, Sato K, Yamamoto S, Matsuyama N, Shimohama T, Matsunaga A, Obuchi S, Shiba Y, Shimizu S, Izumi T. Sympathetic nervous activity and myocardial damage immediately after subarachnoid hemorrhage in a unique animal model. Stroke. 2002;33:1671-1676.
- Kwon KY, Jeon BC. Cytokine levels in cerebrospinal fluid and delayed ischemic deficits in patients with aneurysmal subarachnoid hemorrhage. J Korean Med Sci. 2001;16:774-780.
- Frangiskakis JM, Hravnak M, Crago EA, Tanabe M, Kip KE, Gorcsan J, 3rd, Horowitz MB, Kassam AB, London B. Ventricular arrhythmia risk after subarachnoid hemorrhage. Neurocriti Care. 2009;10:287-294.
- Kopelnik A, Zaroff JG. Neurocardiogenic injury in neurovascular disorders. Crit Care Clin. 2006;22:733-752.
- Hachinski VC, Oppenheimer SM, Wilson JX, Guiraudon C, Cechetto DF. Asymmetry of sympathetic consequences of experimental stroke. Arch Neurol. 1992;49:697-702.
- Colivicchi F, Bassi A, Santini M, Caltagirone C. Cardiac autonomic derangement and arrhythmias in right-sided stroke with insular involvement. Stroke. 2004;35:2094-2098.
- Jauch EC, Saver JL, Adams HP, Jr., Bruno A, Connors JJ, Demaerschalk BM, Khatri P, McMullan PW, Jr., Qureshi AI, Rosenfield K, Scott PA, Summers DR, Wang DZ, Wintermark M, Yonas H. for the early management of patients with acute ischemic stroke: A guideline for healthcare professionals from the american heart association/american stroke association. Stroke. 2013;44:870-947.
|
|
|