|
|
International Journal of Arrhythmia 2014;15(4): 27-34.
|
 |
| MAIN TOPIC REVIEWS |
전극도자 절제술과
변화된 국내 보험 규정 |

|
|
 |
 |
서론
심방세동 환자를 대상으로 하는 새로운 약제, 새로운 치료법의 개발로 심방세동 가이드라인이 자주 업데이트
되고 있다. 이에 전극도자 절제술 부문은 최근 가이드라인에서 어떤 면들이 새롭게 언급되고 있으며,
지난 6월에 개정된 국내 건강보험 요양급여 인정 기준은 어떤지에 대해 알아보고자 한다.
ESC (European Society of Cardiology) 2012년 가이드라인 업데이트1
1. 새로운 증거들
동리듬 유지 측면에서 항부정맥제보다는 전극도자 절제술의 우수성이 추가적인 연구들(MANTRA-PAF
[Medical ANtiarrhythmic Treatment or
Radiofrequency Ablation in Paroxysmal Atrial
Fibrillation],2 RAAFT-2 [Radiofrequency Ablation vs
Antiarrhythmic Drugs as First-Line Treatment of
Paroxysmal Atrial Fibrillation]3)에서 입증되어 2010년
가이드라인의 권고사항이 공고해졌다. 또한 시술 관련
합병증 발생의 가능성이 낮은 선택된 발작성 심방세동
환자들에서는 리듬 유지를 위한 일차 치료로 전극도자 절제술을 선택할 수 있음이 타당하다는 사실을 다시
한번 피력하고 있다(Figure 1A).

비록 전극도자 절제술이 항부정맥제보다 우수한
치료법이지만 재발률은 상당히 높다. 경험이 많은
센터에서 적절한 환자, 심지어 lone atrial fibrillation
(AF) 환자일지라도 후기에 재발하는 경우가 흔하다.
하지만 재발의 가장 중요한 예측인자는 초기
재발이다.4-7 즉, 초기 재발 상태가 유지되는 것이
나중에 재발하는 경우보다 훨씬 중요하다는 의미이다.
합병증은 유럽 기관을 대상으로 조사한 결과에서
뇌졸중 0.6%, 심낭압전 1.3%, 말초혈관 합병증 1.3%,
심낭염 2%로 나와 이전에 보고되었던 미국 데이터 및
전 세계 설문 조사와 유사한 결과를 보였다. 2005-2008년 사이에 첫 번째 절제술을 받았던 4,156명의
데이터베이스 분석에 따르면 총 합병증 발생률은 5%,
절제술 후 1년 이내의 모든 원인에 의한 입원율은 38.5%
였다.8 무증상의 뇌경색은 4-25%로 다양하게
보고되었는데,9-11 이는 절제술에 사용된 도구의 차이에
기인하는 것으로 추정된다. 비록 무증상 뇌경색의
임상적 의미는 분명하지 않으나 더 안전한 심방세동
절제술 방법의 개발이 필요함은 분명하다.
2. 심부전 환자에서의 절제술
개정된 가이드라인에서는 심부전 환자의 리듬 조절
방법에 동원할 수 있는 항부정맥제로 유일하게
amiodarone만을 권고한다. 심부전 환자의 심방세동
증상 조절을 위해 숙련된 센터에서 전극도자 절제술을
시행하는 것은 하나의 치료 전략이 될 수 있다. 물론
심부전 환자에서는 재발률과 합병증 발생률이 높다는
사실은 인지해야 한다. 또한 심방세동의 증상이 심부전
증상과 혼돈될 수 있으므로 주의 깊은 병력 청취가
필요하다. 환자의 증상이 심방세동에 의한 것으로
추정된다면 리듬 조절을 위해 amiodarone과 절제술 중
선택할 수 있다(Figure 1B).
3. 절제술 전후의 항응고요법
절제술 전후의 항응고요법은 뇌졸중 예방 치료가
평생 필요한 환자뿐만 아니라 뇌졸중 위험인자가 없는
환자 모두에게 도움이 되는 것으로 인식되고 있다.
최근에는 시술 직전에 항응고요법을 중지하지 않고
계속 유지하는 방법이 안전하다는 보고가 있었으며,12-15
HRS/EHRA/ECAS (Heart Rhythm Society/European
Heart Rhythm Association/European Cardiac
Arrhythmia Society) 합의문에서도 항응고요법을
중지하고 heparin을 사용하는 방법 대신 항응고요법을
중지하지 않고 계속 투여하는 방법으로 사용할 수
있다고 권고한 바 있다.16 ESC도 이번 가이드라인에서는
항응고요법을 중지하지 않고, 계속 투여하는 방법을
사용할 수 있다고 권고하고 있으며, 절제술 과정 중 INR
(international normalized ratio)은 2.0-2.5 정도를
추천한다. 또한, CHA2DS2-VASc 점수가 2점 이상인
경우에는 시술 성공 여부와 상관없이 장기간의
항응고요법을 권한다. 새로운 항응고제(new oral
anticoagulants, NOAC)에 대해서는 아직 증거가
불충분한 상태여서 강하게 권고하고 있지는 않다.
4. 권고 강도와 증거 수준의 변화
2010년에는 항부정맥제로 리듬 조절에 실패한 발작성
심방세동의 절제술 권고 강도가 class IIa였으나, 이후
축적된 임상 연구 결과들로 인해 2012년에는 class I
으로 격상되었다. 또한 증상이 심하고 위험도가 낮은
환자의 경우 일차 치료로 전극도자 절제술을 고려해야
한다고 권고하고 있다(권고 강도 IIa, 증거 수준 B). 물론
이는 (1) 매우 경험이 풍부한 센터/시술자가 시행하는
경우, (2) 적절하게 환자가 선정된 경우, (3) 다른 치료
대안에 대해서 주의 깊게 평가한 경우, (4) 환자가
선호하는 경우로 한정한다.
지속성 심방세동에 대한 권고안은 2010년에 비해
변환된 것이 없다. 아직까지 무증상의 심방세동 환자에게는
절제술을 권할 만한 증거가 없다.
AHA/ACC/HRS (American Heart Association/
American College of Cardiology/Heart
Rhythm Society) 2014년 가이드라인17
ESC 가이드라인의 주요 업데이트 후 2년 만에 발표된
내용이어서 전극도자 절제술 부문에서는 유럽의 가이드라인과 비교하여 치료 전략에 큰 차이가 없다.
1. 주요 권고사항
I군 또는 III군의 항부정맥제 투여에도 불구하고
증상이 있는 심방세동 환자에서 유형별로 다음과 같이
전극도자 절제술을 권고하고 있다: 발작성(권고 강도 I;
증거 수준 A), 발작성의 일차 치료(권고 강도 IIa; 증거
수준 B), 지속성(권고 강도 IIa; 증거 수준 A), 지속성의
일차 치료(권고 강도 IIb; 증거 수준 C), 장기 지속성(권고 강도 IIb; 증거 수준 B).
아직까지 절제술이 사망률, 뇌졸중, 심부전 등을
줄여줄 수 있는지는 증거가 부족한 상황이다. 이는 현재
진행중인 CABANA (Catheter Ablation vs.
Antiarrhythmic Drug Therapy for Atrial Fibrillation),
EAST (Early Treatment of Atrial Fibrillation for
Stroke Prevention Trial) 연구 등이 증명해줄 수 있을
것으로 기대한다.
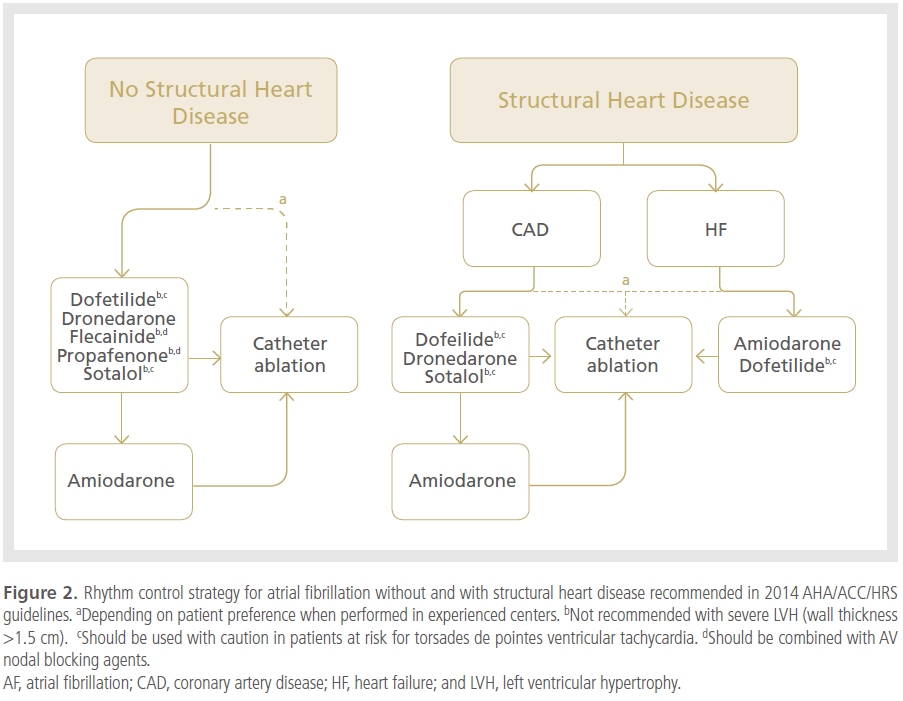
2. 환자의 선정
적절한 환자의 선정을 위해서는 심방세동의 유형,
증상의 정도, 구조적 심장질환이 있는지 등을 평가해야
한다. 리듬 유지 요법에 대한 전략은 ESC 가이드라인과
유사하다(Figure 2).
3. 절제술 전후의 항응고요법
ESC 가이드라인과 마찬가지로 항응고요법 중지 후
heparin 사용의 대안으로 계속해서 항응고요법을
유지하는 전략에 대해 언급을 하고 있다. 하지만 주요
권고사항에는 포함되어 있지 않다. NOAC, 특히
dabigatran에 대한 언급이 있으나 역시 권고사항에는
들어가 있지 않다. 시술 후 장기간 항응고요법에 대한
의견도 ESC 가이드라인과 유사하다. 즉, 위험도가 낮지
않은 군에 대한 항응고요법 중지에 대해서는 신중한
입장이다.
4. 심부전 환자의 절제술
역시 ESC 가이드라인과 유사한 의견을 피력하고
있다. 환자를 전체적으로 잘 파악해서 진행한다면 심한
좌심실 기능부전이 있는 환자에서도 증상이 있는
심방세동을 치료하는 데 절제술이 유용할 수 있다는
내용이다.
5. 합병증
알려진 합병증들에 대한 요약은 Table 1과 같다.
합병증 발생률과 연관된 인자들은 고령, 여성, CHADS2
점수 ≥2이다.8,18,19 또한 ESC 업데이트 가이드라인에도
언급되었듯이 좌심방의 절제술은 MRI로 발견할 수
있는 무증상의 작은 뇌경색을 유발시킬 수 있다. 하지만
대부분은 시간이 경과하면서 해결되거나 사라지는
것으로 보인다.

국내 보험 규정
1. 전극도자 절제술
심방세동 전극도자 절제술의 국내 건강보험
요양급여는 2014년 6월부터 다음과 같은 기준의 적용을
받고 있다.
|
(1)
|
항부정맥 약제(class Ⅰ 또는 class Ⅲ) 중 1가지 이상을
6주 이상 충분한 용량으로 투여한 이후에도 증상이 조절되지 않는 심방세동으로 약제 투여 전후
심전도 검사에서 심방세동이 증명된 경우. 다만,
영구형(permanent) 심방세동은 인정하지 아니함
|
|
(2)
|
항부정맥 약제에 대한 부작용 또는 동결절
기능부전을 동반한 빈맥-서맥 증후군에서와 같이
약제 유지가 불가능한 심방세동으로서 심전도에
의해 확인된 경우
|
|
(3)
|
재시술은 이전 시술 후 3개월이 경과된 이후에
실시하되 심전도상 심방세동 또는 심방빈맥의
재발이 증명된 경우
|
|
(4)
|
심방세동 고주파 절제술 시 CTI (cavotricuspid
isthmus)-dependent 심방조동이 유도된 경우
|
2. 3차원 매핑
3차원 매핑도 2014년 6월부터 요양급여가 인정되고
있다. 기준을 요약하면 3차원 빈맥 지도화를 이용한
심방세동의 고주파 절제술은 요양급여를 인정하며, 3차원 빈맥 지도화를 위해 실시한 영상 진단(CT, MRI)은
별도 요양급여를 인정한다.
결론
최근 가이드라인에서의 주요 이슈는 (1) 전극도자
절제술의 유용성이 더욱 입증되었으며, (2) 일부 발작성
심방세동 환자에게는 일차 치료법으로 절제술을
선택하는 것이 가능하고, (3) 시술 전후 항응고요법을
지속하는 방법이 대두되고 있다는 점 등이다.
가이드라인으로 채택되기 위해 증거가 더 확보되어야
하는 부문은 (1) 전극도자 절제술이 사망률과 뇌졸중을
줄일 수 있는 치료법으로 인정받을 수 있을 것인가, (2)
새로운 항응고제(NOAC)의 시술 전후 사용 지침, (3)
시술과 관련된 합병증을 줄일 수 있는 좀 더 안전한
방법의 개발 등이 될 것이다.
국내에서도 최근 요양급여 인정 기준이 개정되어
심방세동 환자들뿐만 아니라 임상의들의 진료에도 큰
도움이 되고 있다. 빠르게 발전하는 치료법과
가이드라인에 발맞춰 국내 보험 인정 기준도 계속해서
국제적인 수준으로 업데이트될 수 있기를 바란다.
References
- Camm AJ, Lip GY, De Caterina R, Savelieva I, Atar D, Hohnloser SH, Hindricks G, Kirchhof P and Guidelines ESCCfP. 2012 focused update of the ESC Guidelines for the management of atrial fibrillation: an update of the 2010 ESC guidelines for the management of atrial fibrillation. Developed with the special contribution of the European Heart Rhythm Association.
Eur Heart J. 2012;33:2719-2747.
- Cosedis Nielsen J, Johannessen A, Raatikainen P, Hindricks G, Walfridsson H, Kongstad O, Pehrson S, Englund A, Hartikainen J, Mortensen LS and Hansen PS. Radiofrequency ablation as initial therapy in paroxysmal atrial fibrillation.
N Engl J Med. 2012;367:1587-1595.
- Morillo CA, Verma A, Connolly SJ, Kuck KH, Nair GM, Champagne J, Sterns LD, Beresh H, Healey JS, Natale A and Investigators R-. Radiofrequency ablation vs antiarrhythmic drugs as first-line treatment of paroxysmal atrial fibrillation (RAAFT-2): a randomized trial.
JAMA. 2014;311:692-700.
- Arya A, Hindricks G, Sommer P, Huo Y, Bollmann A, Gaspar T, Bode K, Husser D, Kottkamp H and Piorkowski C. Long-term results and the predictors of outcome of catheter ablation of atrial fibrillation using steerable sheath catheter navigation after single procedure in 674 patients.
Europace. 2010;12:173-180.
- Lellouche N, Jais P, Nault I, Wright M, Bevilacqua M, Knecht S, Matsuo S, Lim KT, Sacher F, Deplagne A, Bordachar P, Hocini M and Haissaguerre M. Early recurrences after atrial fibrillation ablation: prognostic value and effect of early reablation.
J Cardiovasc Electrophysiol. 2008;19:599-605.
- Oral H, Knight BP, Ozaydin M, Tada H, Chugh A, Hassan S, Scharf C, Lai SW, Greenstein R, Pelosi F, Jr., Strickberger SA and Morady F. Clinical significance of early recurrences of atrial fibrillation
after pulmonary vein isolation.
J Am Coll Cardiol. 2002;40:100-104.
- Pokushalov E, Romanov A, Corbucci G, Bairamova S, Losik D, Turov A, Shirokova N, Karaskov A, Mittal S and Steinberg JS. Does atrial fibrillation burden measured by continuous monitoring during the blanking period predict the response to ablation at 12-month follow-up?
Heart Rhythm. 2012;9:1375-1379.
- Shah RU, Freeman JV, Shilane D, Wang PJ, Go AS and Hlatky MA. Procedural complications, rehospitalizations, and repeat procedures after catheter ablation for atrial fibrillation.
J Am Coll Cardiol. 2012;59:143-149.
- Di Biase L, Burkhardt JD, Mohanty P, Sanchez J, Horton R, Gallinghouse GJ, Lakkireddy D, Verma A, Khaykin Y, Hongo R, Hao S, Beheiry S, Pelargonio G, Dello Russo A, Casella M, Santarelli P, Santangeli P, Wang P, Al-Ahmad A, Patel D, Themistoclakis S, Bonso A, Rossillo A, Corrado A, Raviele A, Cummings JE, Schweikert RA, Lewis WR and Natale A. Periprocedural stroke and management of major bleeding complications in patients undergoing catheter ablation of atrial fibrillation: the impact of periprocedural therapeutic international normalized ratio.
Circulation. 2010;121:2550-2556.
- Gaita F, Leclercq JF, Schumacher B, Scaglione M, Toso E, Halimi F, Schade A, Froehner S, Ziegler V, Sergi D, Cesarani F and Blandino A. Incidence of silent cerebral thromboembolic lesions after atrial fibrillation ablation may change according to technology used: comparison of irrigated radiofrequency, multipolar nonirrigated catheter and cryoballoon.
J Cardiovasc Electrophysiol. 2011;22:961-968.
- Herrera Siklody C, Deneke T, Hocini M, Lehrmann H, Shin DI, Miyazaki S, Henschke S, Fluegel P, Schiebeling-Romer J, Bansmann PM, Bourdias T, Dousset V, Haissaguerre M and Arentz T. Incidence of asymptomatic intracranial embolic events after pulmonary vein isolation: comparison of different atrial fibrillation ablation technologies in a multicenter study.
J Am Coll Cardiol. 2011;58:681-688.
- Gautam S, John RM, Stevenson WG, Jain R, Epstein LM, Tedrow U, Koplan BA, McClennen S and Michaud GF. Effect of therapeutic INR on activated clotting times, heparin dosage, and bleeding risk during ablation of atrial fibrillation.
J Cardiovasc Electrophysiol. 2011;22:248-254.
- Gopinath D, Lewis WR, Di Biase L and Natale A. Pulmonary vein antrum isolation for atrial fibrillation on therapeutic coumadin: special considerations.
J Cardiovasc Electrophysiol. 2011;22:236-239.
- Hakalahti A, Uusimaa P, Ylitalo K and Raatikainen MJ. Catheter ablation of atrial fibrillation in patients with therapeutic oral anticoagulation treatment.
Europace. 2011;13:640-645.
- Page SP, Siddiqui MS, Finlay M, Hunter RJ, Abrams DJ, Dhinoja M, Earley MJ, Sporton SC and Schilling RJ. Catheter ablation for atrial fibrillation on uninterrupted warfarin: can it be done without echo guidance?
J Cardiovasc Electrophysiol. 2011;22:265-270.
- Calkins H, Kuck KH, Cappato R, Brugada J, Camm AJ, Chen SA, Crijns HJ, Damiano RJ, Jr., Davies DW, DiMarco J, Edgerton J, Ellenbogen K, Ezekowitz MD, Haines DE, Haissaguerre M, Hindricks G, Iesaka Y, Jackman W, Jalife J, Jais P, Kalman J, Keane D, Kim YH, Kirchhof P, Klein G, Kottkamp H, Kumagai K, Lindsay BD, Mansour M, Marchlinski FE, McCarthy PM, Mont JL, Morady F, Nademanee K, Nakagawa H, Natale A, Nattel S, Packer DL, Pappone C, Prystowsky E, Raviele A, Reddy V, Ruskin JN, Shemin RJ, Tsao HM and Wilber D. 2012 HRS/EHRA/ECAS expert consensus statement on catheter and surgical ablation of atrial fibrillation: recommendations for patient selection, procedural techniques, patient management and follow-up, definitions, endpoints, and research trial design.
Europace. 2012;14:528-606.
- January CT, Wann LS, Alpert JS, Calkins H, Cleveland JC, Jr., Cigarroa JE, Conti JB, Ellinor PT, Ezekowitz MD, Field ME, Murray KT, Sacco RL, Stevenson WG, Tchou PJ, Tracy CM and Yancy CW. 2014 AHA/ACC/HRS guideline for the management of patients with atrial fibrillation: A report of the American College of Cardiology/American Heart Association task force on practice guidelines and the Heart Rhythm Society.
Circulation. 2014.
- Hoyt H, Bhonsale A, Chilukuri K, Alhumaid F, Needleman M, Edwards D, Govil A, Nazarian S, Cheng A, Henrikson CA, Sinha S, Marine JE, Berger R, Calkins H and Spragg DD. Complications arising from catheter ablation of atrial fibrillation: temporal trends and predictors.
Heart Rhythm. 2011;8:1869-1874.
- Piccini JP, Sinner MF, Greiner MA, Hammill BG, Fontes JD, Daubert JP, Ellinor PT, Hernandez AF, Walkey AJ, Heckbert SR, Benjamin EJ and Curtis LH. Outcomes of Medicare beneficiaries undergoing catheter ablation for atrial fibrillation.
Circulation. 2012;126:2200-2207.
|
|
|