유두근 심실빈맥
Abstract
The papillary muscles are potential sites of reentry that may contribute to the maintenance of ventricular arrhythmia in animal models. Recently, the papillary muscles in the left ventricle have been reported as an arrhythmogenic focus in patients with and without structural heart disease. Over recent decades, the introduction of new catheter ablation technology has led to improvements in treatment, and catheter ablation is often curative for idiopathic ventricular tachycardia, including papillary muscle ventricular tachycardia. This review discusses the current knowledge of ventricular tachycardia originating from the papillary muscles, and explores recent advances in ablation techniques.
Key words: Papillary Muscle; Ventricular Tachycardia; Catheter Ablation
서론
유두근(papillary muscle, PM)은 전기적으로 활동적인 조직이기 때문에 reentry가 일어날 수 있으며, 심실빈맥 및 심실세동이 지속되는 데에 기여한다는 것이 동물 실험에서 보고되었다[ 1]. 이후 2008년 Doppalapudi 등이 처음으로 구조적 심질환이 없는 환자에서 후내측 유두근(postero-medial PM)에서 기인하는 특발성 심실빈맥을 보고하였다[ 2]. 현재 좌심실의 유두근에서 기인하는 심실빈맥은 특발성 심실부정맥의 한 종류로 따로 분류가 되고 있으며 빈도는 약 7% 정도로 보고 되고 있다[ 3]. 두 개의 승모판막은 좌심실의 앞쪽(antero-lateral PM)과 뒤쪽(postero-medial PM)으로 각각 연결이 되어 있다. 유두근에서 유발하는 심실빈맥은 후내측 유두근에서 유발하는 경우가 훨씬 흔하다. 심전도에서 모양은 우각차단 형태를 나타내며, 후내측 유두근에서 유발하는 경우에는 frontal plane에서 superior axis 형태를 보이며[ 2], 전외측 유두근(antero-lateral PM)에서 유발하는 경우에는 inferior axis 형태를 보이는 경우가 많았다( Figure 1) [ 4].
섬유속 심실빈맥과의 비교 분석
유두근은 해부학적으로 전도 시스템에 관여하는 구조물인 좌심실의 섬유속과 인접해 있어 섬유속 심실빈맥(fascicular ventricular tachycardia)과의 감별진단이 필요하며, 몇몇 연구가 발표되었다( Table 1). 유두근에서 기인하는 심실빈맥의 경우 환자 연령이 더 많았다[ 5]. 유두근 심실빈맥은 대개 focal, non-reentrant 기전을 가지기 때문에 지속성 심실빈맥보다는 조기심실수축 또는 비지속성 심실빈맥의 형태로 많이 나타나며, 전기생리학 검사 도중 인위적인 전기 자극(programmed electrical stimulation)으로는 유발되지 않았다[ 2]. 대신 자발적으로 발생하거나 isoproterenol 또는 epinephrine 주입으로 유발되는 경우가 많았다. 해부학적으로 인접해 있기 때문에 심전도에서 모양이 비슷하게 나타날 수 있으나, QRS 너비가 유두근 심실빈맥의 경우 훨씬 컸다(150±15 msec vs. 127±11 msec) [ 3]. 세부적인 심전도 모양으로 lead V1의 경우 유두근 심실빈맥에서는 qR 또는 R 형태인 경우가 많으나 섬유속 심실빈맥의 경우에는 rsR’인 경우가 많았다. 또한 유두근 심실빈맥에서는 lead I과 aVL에서 Q wave가 없는 경우가 많았다[ 3]. 유두근 심실빈맥의 QRS의 모양이 약간씩 변할 수 있는데, 이는 유두근 내부의 복잡한 구조물 내에서 다양한 exit site로 인해 나타날 수 있다.
치료
유두근 심실빈맥은 섬유속 심실빈맥과 다르게 verapamil에 효과가 없었으며, class IC 항부정맥 약제에도 효과가 없는 경우가 많았다[ 4]. 특발성 심실부정맥 중에서 모양이 단일형(monomorphic)이면서 심한 증상을 유발하거나 부정맥 약제에 효과가 없는 경우 최근에 전극도자절제술이 많이 행해지고 있으며, 유두근 심실빈맥에서도 근치적 치료로 전극도자절제술이 많이 시도되고 있다. 시술 방법으로는 activation mapping이 유용했으며, pacemapping도 도움이 되었다. 하지만 유두근에 카테터를 안정적으로 접근하기가 쉽지가 않으며, 유발 부위가 심내막이 아니라 유두근의 깊은 내부인 경우가 많기 때문에 pacemapping이 잘 맞지 않는 경우도 있었다[ 6]. 섬유속 심실빈맥에서는 성공적인 시술 부위에서 항상 Purkinje 전위(potential)가 보였지만 유두근 심실빈맥에서는 전도 시스템이 관여하지 않기 때문에 보이지 않는 경우가 많았다[ 2, 3]. 동리듬 중에 Purkinje 전위가 보인다 하더라도 심실부정맥이 발생했을 때에는 섬유속 심실빈맥과 같이 Purkinje 전위가 선행하는 것이 아니라 심실 근육에서 기인하는 전위(ventricular potential)가 선행한다고 보고하였다( Figure 2) [ 2]. 또한 Purkinje 시스템이 관여하지 않기 때문에 정상 동리듬 중에는 이완기 전위가 나타나지 않는 경우가 대부분이었다[ 4]. 또한 심실부정맥이 있을 때에 선행하는 심실 전위가 클수록 전극도자절제술의 성공률이 높았는데, 이는 부정맥을 유발하는 부위와의 근접성이 높기 때문인 것으로 생각된다[ 7]. 다른 연구에서는 Purkinje 전위가 보일수록 성공률이 높았다고 하며, 전극도자절제술이 실패한 군에서 심장 자기공명영상촬영에서 측정한 유두근의 무게가 더 컸다[ 6]. 유두근의 해부학적 구조 및 심장이 수축하는 특징, 카테터의 불안정성 등으로 인해 전극도자절제술은 쉽지 않은 경우가 많다. 또한 유두근 아래쪽의 심근은 대개 두꺼워 실제로 부정맥이 유발되는 부위가 심장내막에서 거리가 상당히 먼 경우가 많이 때문에 고주파 전극도자절제술로 충분히 깊은 병변을 만들기 어려운 경우가 많다. 따라서 섬유속 심실빈맥에 비해 성공률이 낮은 편으로 보고되고 있다[ 4]. 대안으로 irrigated-tip 카테터 또는 8 mm-tip 카테터 등을 사용하여 에너지를 30 W부터 시작해서 점차적으로 50 W까지 상향 조정하면서 저항(impedance)이 8-10 ohm 낮아지는지, 최대 온도가 40℃에 도달하는지 등을 살펴보는 방법이 있다[ 2]. 하지만 steam pop 또는 심장 내 천공에 대한 주의가 필요하다. 고주파 에너지 전달 도중 부정맥이 유발이 되면서 카테터의 안정성이 떨어지는 경우가 많은데, 이때 빈맥의 주기보다 좀 더 빠르게 우심실을 자극하면 카테터의 안정성에 도움을 줄 수 있다[ 6]. 또한 심장 내 초음파(intra-cardiac echocardiography)의 사용이 카테터의 위치를 확인하는 데 도움을 줄 수 있다( Figure 3). 시술 후에는 승모판막 역류가 발생하지 않았는지 심장 초음파 검사를 시행해서 체크해 보아야 한다[ 4].
결론
좌심실의 유두근에서 기인하는 심실부정맥은 특발성 심실부정맥의 한 종류로 빈도는 약 7% 정도로 보고되고 있다.
심전도에서 우각차단 형태를 나타내며, 조기심실수축 또는 비지속성 심실빈맥으로 많이 나타난다. 치료로 전극도자 절제술을 시행할 수 있으며, activation mapping 또는 pacemapping이 유용하고, 심장 내 초음파의 사용이 성공률을 높일 수 있다. 하지만 유두근의 수축하는 특징, 카테터의 불안정성 등으로 인해 아직까지 성공률에는 제한이 있으며, 향후 더 나은 전극도자절제술 결과를 위해서는 새로운 테크닉의 개발 및 연구가 필요하다.
References
1. Kim YH, Xie F, Yashima M, Wu TJ, Valderrabano M, Lee MH, Ohara T, Voroshilovsky O, Doshi RN, Fishbein MC, Qu Z, Garfinkel A, Weiss JN, Karagueuzian HS, Chen PS. Role of papillary muscle in the generation and maintenance of reentry during ventricular tachycardia and fibrillation in isolated swine right ventricle. Circulation 1999; 100: 1450-1459.   2. Doppalapudi H, Yamada T, McElderry HT, Plumb VJ, Epstein AE, Kay GN. Ventricular tachycardia originating from the posterior papillary muscle in the left ventricle: a distinct clinical syndrome. Circ Arrhythm Electrophysiol 2008; 1: 23-29.   3. Good E, Desjardins B, Jongnarangsin K, Oral H, Chugh A, Ebinger M, Pelosi F, Morady F, Bogun F. Ventricular arrhythmias originating from a papillary muscle in patients without prior infarction: a comparison with fascicular arrhythmias. Heart Rhythm 2008; 5: 1530-1537.   4. Yamada T, McElderry HT, Okada T, Murakami Y, Doppalapudi H, Yoshida N, Allred JD, Murohara T, Kay GN. Idiopathic focal ventricular arrhythmias originating from the anterior papillary muscle in the left ventricle. J Cardiovasc Electrophysiol 2009; 20: 866-872.   5. Yamada T, Doppalapudi H, McElderry HT, Okada T, Murakami Y, Inden Y, Yoshida Y, Kaneko S, Yoshida N, Murohara T, Epstein AE, Plumb VJ, Kay GN. Idiopathic ventricular arrhythmias originating from the papillary muscles in the left ventricle: prevalence, electrocardiographic and electrophysiological characteristics, and results of the radiofrequency catheter ablation. J Cardiovasc Electrophysiol 2010; 21: 62-69.   6. Yokokawa M, Good E, Desjardins B, Crawford T, Jongnarangsin K, Chugh A, Pelosi F, Jr., Oral H, Morady F, Bogun F. Predictors of successful catheter ablation of ventricular arrhythmias arising from the papillary muscles. Heart Rhythm 2010; 7: 1654-1659.    7. Ban JE, Lee HS, Lee DI, Park HC, Park JS, Nagamoto Y, Choi JI, Lim HE, Park SW, Kim YH. Electrophysiological characteristics related to outcome after catheter ablation of idiopathic ventricular arrhythmia originating from the papillary muscle in the left ventricle. Korean Circ J 2013; 43: 811-818.   
Figure 1.
VT originating from postero-medial PM exhibited a right bundle branch block with superior axis QRS morphology (A) while VT from antero-lateral PM exhibited a right bundle branch block with inferior axis QRS morphology (B).
PM, papillary muscle; VT, ventricular tachycardia
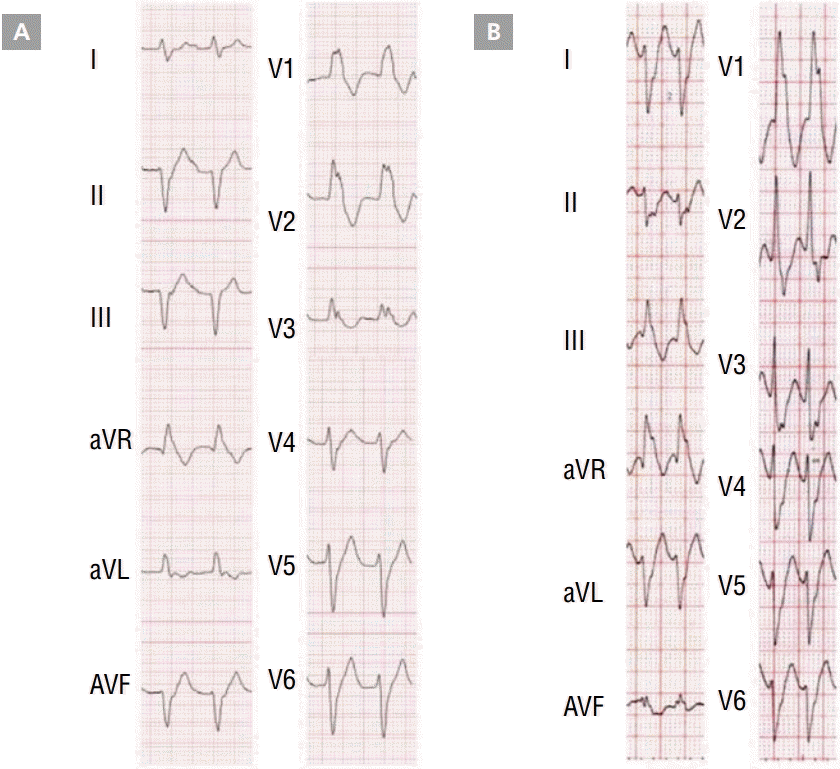
Figure 2.
Activation mapping showing bipolar electrograms from distal bipoles of the ablation catheter (ABL d) at the site of earliest local activation during VT. The local ventricular electrogram recorded from the distal bipole of the ablation catheter preceded the onset of QRS by 30 msec. RF ablation at this site successfully terminated VT. During VT, high-frequency potentials likely representing the Purkinje network (red arrows) were recorded. However, it was not the earliest potential, suggesting that the conduction system was not directly involved in the tachycardia.
I, III, V1, and V4 are surface ECG leads; ABL d and ABL p are distal and proximal bipolar electrograms from the ablation catheter; His d, His m, and His p are proximal, mid, and distal bipolar His-bundle electrograms; and LV 1/2 through to 11/12 are bipolar electrograms recorded from the left ventricle, with the LV 3/4 pair located at the antero-lateral PM.
ECG, electrocardiogram; LV, left ventricle; PM, papillary muscle; RF, radiofrequency; VT, ventricular tachycardia.
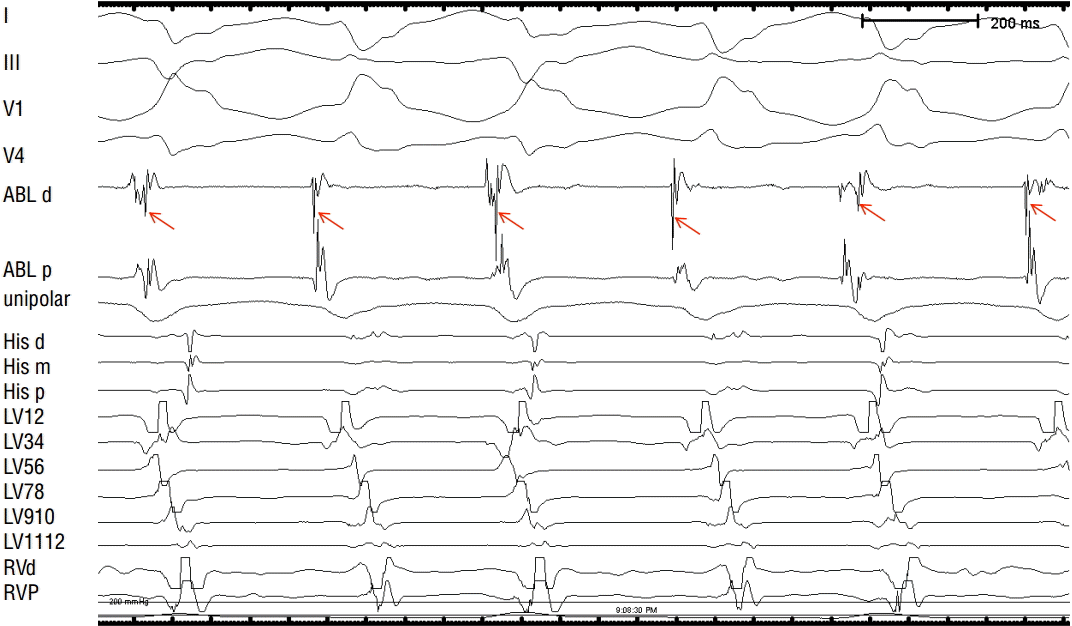
Figure 3.
Intra-cardiac echocardiographic image of the successful ablation site. A 2-dimensional intra-cardiac echocardiographic image demonstrating that the ablation catheter was positioned at the ALPM.
ALPM, antero-lateral papillary muscle; LV, left ventricle.
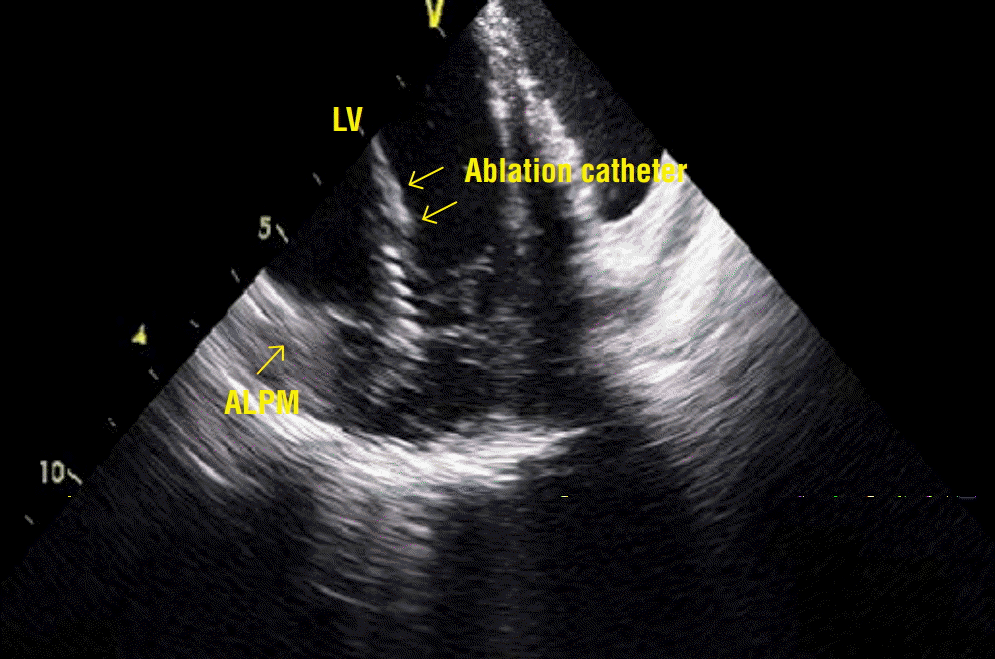
Table 1.
Comparison of clinical, electrocardiographic and electrophysiological characteristics between PM VT and fascicular VT
|
PM VT |
Fascicular VT |
|
Manifestation of arrhythmia |
Sustained VT<PVC or non-sustained VT |
PVC or non-sustained VT<Sustained VT |
|
Mechanism |
Abnormal automaticity or triggered activity |
Re-entrant |
|
ECG during arrhythmia |
|
|
|
QRS morphology |
RBBB |
RBBB |
|
QRS duration |
Longer |
Shorter |
|
V1 |
qR or R |
rsR' |
|
Q wave in limb leads |
(-) |
(+) |
|
Response to verapamil |
(-) |
(+) |
|
Induction mode during EPS |
Spontaneously or during an infusion of isoproterenol or epinephrine |
Programmed electrical stimulation |
|
Recurrence rate after RFCA |
Relatively high |
Low |
|
High frequency potential preceding the earliest local ventricular electrogram |
(-) |
(+) |
|
|
















